Tubuläre Gewebe mit rigiden und flexiblen Strukturzonen und Stofftrans-port zum biomimetischen Aufbau der Trachea
Fabrics Smart Textiles Medicine
Abstract
Die erfolgreiche Therapie von Verletzung der Trachea (Luftröhre) stellt eine immense Herausforderung dar und hat eine große gesellschaftliche und medizinische Relevanz. Jede Behandlung und anschließende Versorgung der Trachea mit einem Stoma führen zu funktionellen Nachteilen wie der Befeuchtung der Atemluft, schlechterem Geruchs- und Geschmackssinn oder fehlerhafte Stimmbildung. Ein weiterer Nachteil ist, dass bis zu 20 % der Patienten an einer Stenose (Verengung) der Trachea leiden [1]. Im Rahmen des interdisziplinären IGF-Forschungsprojektes 01IF22889N des ITM wurde deshalb ein integral gefertigtes, textiles, druckstabiles biomimetisches Tracheaimplantat entwickelt.
Report
Ausgangssituation und Problemstellung
Die Luftröhre (Trachea) erfüllt zwei Hauptfunktionen: (I) Realisierung des luftdichten und mechanisch stabilen Übergangs vom Kehlkopf zum Bronchialbaum der Lunge für den Lufttransport und (II) Erleichterung des Schleimabtransports. Funktion (I) übernimmt. eine röhrenförmige Konstruktion aus Knorpelspangen und Längsmuskeln, die für die seitliche Stabilität sowie die Längsflexibilität sorgen. Auf diese Weise wird das Lumen für die Atemluft offengehalten. Zusätzlich wird beim Einatmen die Atemluft angefeuchtet und erwärmt. Funktion (II) ist ein Reinigungsmechanismus, der durch eine besondere Schleimhautschicht (mukoziliäre respiratorische Epithelschicht) erfüllt wird. Hierbei übernehmen schleimproduzierende Zellen und Zellen mit Flimmerhärchen (Zilien) auf der Oberfläche den Transport von Schleim und Partikeln [2].
Nach einer Verletzung der Trachea sind diese Funktionen durch das Einsetzen einer Trachealkanüle beeinträchtigt. So werden in Deutschland jährlich 53.000 Trachearesektionen (Ersetzen eines Teils der Trachea) durchgeführt [3]. Ein hoher Anteil, etwa 40.000 Patienten erhalten dabei eine außerklinische Versorgung durch eine operativ geschaffene Öffnung in der Luftröhre, ein sogenanntes Stoma [3]. Diese Versorgung ist mit erheblichen Nachteilen verbunden: 1. einer schlechteren Befeuchtung und Erwärmung der Atemluft, 2. eines schlechteren Geruchs- und Geschmackssinns, 3. einer fehlerhaften Stimmbildung, und 4. einer Verengung der Luftröhre.
Der Gold-Standard für die Rekonstruktion der Trachea ist die End-to-End Anastomose, bei der ein Teil der Luftröhre entfernt und die verbleibenden Enden miteinander vernäht werden [4]. Für die Anwendung muss aber bei Erwachsenen mindestens die Hälfte und bei Kindern ein Drittel der Trachea vorhanden bleiben, da die Operation sonst nicht durchgeführt werden kann [5]. Trotzdem treten in bis zu 20 % der operierten Fälle Komplikationen auf [6]. Da auf die vernähten Tracheaenden große Kräfte wirken, kann dies zum Ausreißen der Naht und zu einer Verschiebung der Luftröhre in den Brustraum führen. Auch besteht die Gefahr, dass die Enden nicht richtig zusammenwachsen und es zu narbigen Verengungen der Luftröhre, Luftröhrenentzündungen, Heiserkeit, Stimmverlust und Lähmung der Stimmlippennerven sowie Schluckstörungen kommt [7]. Bisher untersuchte Ansätze – darunter synthetische Implantate, Konstrukte aus patienteneigenem Gewebe, Spendertracheen und Tissue-Engineering-Verfahren – konnten bislang keine funktionsfähige Zilienschicht für den Schleim- und Partikeltransport nachbilden. Weder diese fehlende Transportfunktion noch die hohe Komplikationsrate und der Mangel an geeignetem Spendergewebe erlauben aktuell einen verlässlichen Einsatz bei größeren Tracheadefekten nach einer klinisch notwendigen Resektion. Deshalb steht derzeit kein Implantat als adäquater Tracheaersatz zur Verfügung.
Somit ist es notwendig, neuartige Implantate zu entwickeln, die sowohl die mechanische Stabilität, als auch die innere Transportfunktion der natürlichen Trachea nachahmen. Ziel des durchgeführten IGF-Projekts war es deshalb ein textiles, funktionelles und biomimetisches Schlauchgewebe zu entwickeln. Dieses Gewebe sollte eine zilienähnliche Struktur für den aktiven Stofftransport aufweisen. Gleichzeitig sollten rigide, 3D-gedruckte Stützstrukturen, die bereits während des Webprozesses integriert werden können, das Schlauchgewebe vor einem Kollaps schützen. Beide Aspekte dienen dazu, fehlendes oder entferntes Tracheagewebe sicher zu überbrücken. Die Zilienbewegung sollte hierbei durch elektroaktive piezoelektrische PVDF-Fasern realisiert werden, die in Form von Polnoppen in das Gewebe integriert wurden. Die Aktivierung der Zilienbewegung soll hierbei durch den piezoelektrischen Effekt erfolgen, der durch das erzeugte elektrische Feld von stromdurchflossenen Leitern aktiviert wurde.
Entwicklung tubulärer Gewebestrukturen
Zur Herstellung eines tubulären Gewebes mit Zilien an der Gewebeoberfläche wurden verschiedene Varianten für ein mehrlagiges Gewebe mit in das Schlauchinnere zeigende Polschlaufen entwickelt. Die Gewebe wurden mittels marktverfügbarer Spulenschützenwebmaschinentechnologie unter Verwendung einer Jacquardeinheit für eine vielseitige Anpassung der Gewebestruktur gefertigt.
Die schlauchförmige Grundstruktur wurde aus Polyesterfäden gewebt. Je nach Variante wurden Zilienfäden bzw. eine Kombination aus Zilienfäden (piezoelektrisches PVDF oder Nitinol-Fäden) und Leiterfäden (besilbertes Polyamid, Madeira HC40) in das Grundgewebe eingebunden. Der Einsatz von Leiterfäden war bei Verwendung von elektroaktiven PVDF-Multifilamentfäden oder Kurzfasern nötig, um die Zilienbewegung anzuregen. Beim Einsatz von Ein- bzw. Zwei-Weg-Formgedächtnis (FG)-Fäden als Zilienmaterial waren keine separaten Leiterfäden in das Gewebe einzubinden, da die FG-Fäden direkt kontaktiert wurde und leitfähig waren, um die Bewegung der Zilien einzuleiten.
Entwicklung biomimetischer Stützstrukturen
Die menschliche Luftröhre besitzt etwa 15 bis 20 Trachealknorpel. Sie sind hufeisenförmig, haben einen Durchmesser von 20 mm, wobei die offene Seite nach dorsal (zum Rücken gewandt) weist, und etwa 4 mm breit und 1 mm stark ist. Ihre Außenfläche ist plan und die nach innen weisende Oberfläche konvex. Webtechnisch integrierbare Trachealknorpel (Knorpelspangen/Stützstrukturen) sollten mittels 3D-Druck gefertigt werden und sollten einer Kompressionskraft von mind. 1,2 N standhalten.
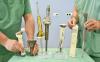
Basierend auf dieser beschriebenen Geometrie wurden insgesamt 10 verschiedene Modelle entwickelt. Die Unterschiede der Geometrien ergaben sich aus der Variation in der Schenkelgeometrie (C- und U-förmig), Wandstärke und Radius. Die Erzeugung der Stützstrukturen wurde mittels Photopolymerdruck nach dem Stereolithographiekonzept mit einem Objet 30 Prime, Fa. Stratasys umgesetzt, um die notwendigen Geometriedetails realisieren zu können. Exemplarische Strukturen sind in Abbildung 1 dargestellt.
Zur Untersuchung der Knorpelstrukturen sind anforderungsgerechte Klemmen für marktverfügbare Messtechnik entwickelt, konstruiert und mittels 3D-Druck umgesetzt worden. Die entwickelten Klemmen ermöglichen eine Druckbelastung in verschiedenen anatomischen Lagen der Knorpelspangen (anterior-posterior & medial-lateral).
Integration der Stützstrukturen in die Gewebestruktur
Auf Basis der zuvor vorgestellten Bindung für das Schlauchgewebe inklusive der im Grundgewebe verankerten Schlaufen an der Gewebeoberfläche, wurde eine Bindung entwickelt, welche die entwickelten Stützstrukturen in definierten Abständen im Grundgewebe aufnehmen und fixieren konnte. Die webtechnische Integration der Stützstrukturen wurde durch das Weben einer Gewebetasche über den gesamten Schlauchumfang des Gewebes realisiert. Die Dimensionen (Breite und Dicke) der Gewebetasche wurden an die der Stützstrukturen angepasst, wodurch diese zwischen zwei Gewebelagen fixiert und gegen ein Verrutschen sowie ein „Herausdrehen“ aus der Struktur gesichert wurden. Die Anzahl der Stützstrukturen pro definierter Gewebelänge war bindungstechnisch einstellbar, ebenso konnten unterschiedliche Spangenbreiten durch Anpassung der Gewebetaschengröße in das Schlauchgewebe integriert werden. Der umgesetzte Demonstrator ist in 3 dargestellt. Deutlich erkennbar sind die nach innen zeigenden Zilien und Gewebetaschen mit den integrierten Stützstrukturen.
Textilphysikalische Analyse der Stütz- und Gewebestrukturen sowie Bewegungsanalyse
Die mittlere Reißkraft der menschlichen Luftröhre liegt bei ca. 230 N [8]. Die tubulären Gewebestrukturen mit integrierten Stützstrukturen wiesen eine Maximalzugkraft von ca. 4300 N auf. Dabei ist eine Streckgrenze von ca. 1400 N ermittelt worden. Somit werden die mechanischen Anforderungen der menschlichen Trachea vollständig erfüllt. Alle entwickelten Sützstrukturen zum Vermeiden des Zusammenfallens der Trachea wiesen eine höhere Kompressionskraft als 1,2 N auf. Teilweise wurde der Zielwert um das zehnfach übertroffen.
Darüber hinaus wurde der Einfluss wiederholter bzw. zyklischer Zugbelastung auf die Position der in das Gewebe integrierten Stützstrukturen untersucht. Dazu wurde ein Lastwechselversuch mit 150 Zyklen durchgeführt, bei dem eine Zugbelastung bis zu einer maximalen Kraft von 230 N (Zielkennwert) und eine anschließende Entlastung bis zur Ausgangsposition wiederholt wurde. Hierfür ist eine Probenaufnahme entwickelt und umgesetzt worden, damit die tubuläre Struktur biomimetisch über den gesamten Querschnitt belastet wurde. Die Ergebnisse zeigen, dass die in die Gewebetaschen eingewebten Stützstrukturen stabil fixiert blieben und kein „Herausdrehen“ in Umfangsrichtung auftrat. Die gewählte Integrations- und Fixiermethode gewährleistet somit eine dauerhafte Positionsstabilität unter zyklischer Belastung.
Die Bewegungsanalyse der verschiedenen Muster hat ergeben, dass mittels PVDF-Fasern keine Zilienbewegung ermöglicht wurde. Jedoch konnte mittels der FGL-Fäden mit einem Zwei-Wege-Effekt eine wiederholbare Bewegung der Zilien gezeigt werden. Dieser Ansatz kann zukünftig dazu verwendet werden, die Funktionsweise menschlicher Zilien nachzustellen. Als weiteren alternativen Ansatz wurden Gewebe mit parallelen Leiterfäden mit Polyamid Kurzfasern beflockt. Mittels eines elektrischen Wechselfeldes konnte auch hier eine intermittierende Zilienbewegung nachgestellt werden.
Zusammenfassung
Am ITM wurde ein neuartiges Trachealimplantat entwickelt, welches die makroskopische Struktur der menschlichen Luftröhre hervorragend nachbildet. Die entwickelte Struktur war mittels marktverfügbarer Schützenwebtechnologie ohne eine konstruktive Anpassung herstellbar. Zum Erhalt einer druckstabilen tubulären Struktur sind 3D-gedruckte Stützstrukturen in Gewebetaschen integriert worden. Die Fertigung kann integral erfolgen und ist patientenindividuell anpassbar in Gewebelänge, Stützstrukturabstand, -anzahl und Druckstabilität. Darüber hinaus wurden zur Nachbildung der mikroskopischen Struktur verschiedene Konzepte untersucht, um einen Stofftransport zu erzeugen. Grundlage war die Erzeugung von Polnoppengeweben und der Verwendung von piezoelektrischen PVDF-Fasern. Hierbei hat sich herausgestellt, dass mittels PVDF-Noppen keine Bewegung im mikroskopischen Maßstab erzielbar war. Mittels anderer Aktorfasern wie Nitinolfasern konnte eine Zilienbewegung erzeugt werden. Zudem ist auch mittels Flockfasern eine Zilienbewegung erzeugbar.
Danksagung
Das Projekt „Tubuläre Gewebe mit rigiden und flexiblen Strukturzonen und Stofftrans-port zum biomimetischen Aufbau der Trachea (01IF22889N)“ wird im Rahmen des Programms „Industrielle Gemeinschaftsforschung (IGF)“ durch das Bundesministerium für Wirtschaft und Energie aufgrund eines Beschlusses des Deutschen Bundestages gefördert.
Literaturverzeichnis
[1] Aleksanyan, A. ; Stoelben, E.: Die laryngotracheale Resektion als Alternative zum permanenten Tracheostoma. In: Pneumologie 73 (2019), Nr. 4, S. 211–218. URL https://www.thieme-connect.com/products/ejournals/html/10.1055/a-0809-0232
[2] Udelsman, Brooks ; Mathisen, Douglas J. ; Ott, Harald C.: A reassessment of tracheal substitutes-a systematic review. In: Annals of Cardiothoracic Surgery 7 (2018), Nr. 2, S. 175–182. URL https://www.annalscts.com/article/view/16458/16661
[3] BVMed: BVMed informiert über Tracheotomie- und Laryngektomie-Versorgung. URL https://www.bvmed.de/verband/presse/pressemeldungen/bvmed-informiert-ueber-tracheotomie-und-laryngektomie-versorgung. – Aktualisierungsdatum: 2016-05-19 – Überprüfungsdatum 2025-10-15
[4] Canzano, F. ; Aggazzotti Cavazza, E. ; Mattioli, F. ; Ghidini, A. ; Bottero, S. ; Presutti, L.: Step-by-Step Tracheal Resection with End-to-End Anastomosis. In: Ghidini, Angelo; Mattioli, Francesco; Bottero, Sergio; Presutti, Livio (Hrsg.): Atlas of Airway Surgery : A Step-by-Step Guide Using an Animal Model. Cham : Springer International Publishing, 2017, S. 75–82
[5] Wemer, Richard D. ; Detamore, Michael ; Weatherly, Robert A.: Immunohistochemical characterization of the rabbit tracheal cartilages. In: Journal of Biomedical Science and Engineering 03 (2010), Nr. 10, S. 1007–1013
[6] Damiano, Giuseppe ; Palumbo, Vincenzo Davide ; Fazzotta, Salvatore ; Curione, Francesco ; Lo Monte, Giulia ; Brucato, Valerio Maria Bartolo ; Lo Monte, Attilio Ignazio: Current Strategies for Tracheal Replacement: A Review. In: Life 11 (2021), Nr. 7, S. 618. URL https://www.mdpi.com/2075-1729/11/7/618
[7] Rettinger, Gerhard ; Hosemann, Werner ; Hüttenbrink, Karl-Bernd ; Werner, Jochen Alfred: HNO-Operationslehre : Mit allen wichtigen Eingriffen. 5., vollständig überarbeitete Auflage. Stuttgart : Thieme, 2018
[8] A. Berghaus: Alloplastischer Trachealersatz. In: Herz-, Thorax- und Gefässchirurgie 1987 (1987), Band 1. URL https://epub.ub.uni-muenchen.de/6218/1/6218.pdf – Überprüfungsdatum 2025-10-15
Technische Universität Dresden
Fakultät Maschinenwesen
Institut für Textilmaschinen und Textile Hochleistungswerkstofftechnik (ITM)
01062 Dresden











![Abbildung 3: Zugfestigkeit (Fmax) der Multifilamentgarne aus Chitin gelöst mit EMIMOPr (links); Vergleich der Zugfestigkeiten der Chitinmultifilamentgarne mit Chitosanfasern aus Essigsäure-basiertem Nassspinnpro-zess [11] und mittels IL (EMIMOAc) hergestellten Chitosanfilamentgarnen [12] (rechts)](/sites/default/files/styles/thumbnail/public/2025-06/Abb3.png?itok=zmIRsVko)


