Tubular tissues with rigid and flexible structural zones and mass transport for the biomimetic construction of the trachea
Fabrics Smart Textiles Medicine
Abstract
The successful treatment of tracheal (windpipe) injuries is an immense challenge and has great social and medical relevance. Every treatment and subsequent care of the trachea with a stoma leads to functional disadvantages such as humidification of the air we breathe, poorer sense of smell and taste, or faulty voice formation. Another disadvantage is that up to 20% of patients suffer from stenosis (narrowing) of the trachea [1]. As part of the interdisciplinary IGF research project 01IF22889N of the ITM, an integrally manufactured, textile, pressure-stable biomimetic tracheal implant was therefore developed.
Report
Initial situation and problem definition
The windpipe (trachea) fulfils two main functions: (I) it provides an airtight and mechanically stable passage from the larynx to the bronchial tree of the lungs for air transport, and (II) it facilitates the transport of mucus. Function (I) is performed by a tubular structure consisting of cartilage rings and longitudinal muscles, which provide lateral stability and longitudinal flexibility. This keeps the lumen open for breathing air. In addition, the inhaled air is moistened and warmed. Function (II) is a cleaning mechanism that is performed by a special mucous membrane layer (mucociliary respiratory epithelial layer). Here, mucus-producing cells and cells with tiny hairs (cilia) on their surface transport mucus and particles [2].
After an injury to the trachea, these functions are impaired by the insertion of a tracheal cannula. In Germany, 53,000 tracheal resections (replacement of part of the trachea) are performed annually [3]. A high proportion, around 40,000 patients, receive non-clinical care through a surgically created opening in the windpipe, known as a stoma [3]. This treatment has significant disadvantages: 1. poorer humidification and warming of the inhaled air, 2. poorer sense of smell and taste, 3. impaired voice formation, and 4. narrowing of the windpipe.
The gold standard for tracheal reconstruction is end-to-end anastomosis, in which part of the trachea is removed and the remaining ends are sutured together [4]. However, for this procedure to be performed, at least half of the trachea must remain in adults and one third in children, otherwise the operation cannot be carried out [5]. Nevertheless, complications occur in up to 20% of cases [6]. As the sutured ends of the trachea are subject to considerable force, this can lead to the suture tearing and the trachea shifting into the chest cavity. There is also a risk that the ends will not grow together properly, leading to scarred narrowing of the trachea, tracheitis, hoarseness, loss of voice and paralysis of the vocal cord nerves, as well as swallowing disorders [7]. Approaches investigated to date – including synthetic implants, constructs made from the patient's own tissue, donor tracheas and tissue engineering procedures – have not yet been able to replicate a functional cilia layer for mucus and particle transport. Neither this lack of transport function nor the high complication rate and shortage of suitable donor tissue currently allow for reliable use in cases of larger tracheal defects following clinically necessary resection. As a result, there is currently no implant available that can adequately replace the trachea.
It is therefore necessary to develop novel implants that mimic both the mechanical stability and the internal transport function of the natural trachea. The aim of the IGF project was therefore to develop a textile, functional and biomimetic tubular fabric. This fabric should have a cilia-like structure for active substance transport. At the same time, rigid, 3D-printed support structures, which can be integrated during the weaving process, were to protect the tubular fabric from collapsing. Both aspects serve to safely bridge missing or removed tracheal tissue. The ciliary movement should be achieved by electroactive piezoelectric PVDF fibres integrated into the tissue in the form of polarised naps. The ciliary movement is to be activated by the piezoelectric effect, which is triggered by the electric field generated by current-carrying conductors.
Development of tubular tissue structures
To produce a tubular fabric with cilia on the fabric surface, various variants were developed for a multi-layer fabric with naps pointing into the interior of the tube. The fabrics were manufactured using commercially available shuttle loom technology with a Jacquard unit for versatile adaptation of the fabric structure.
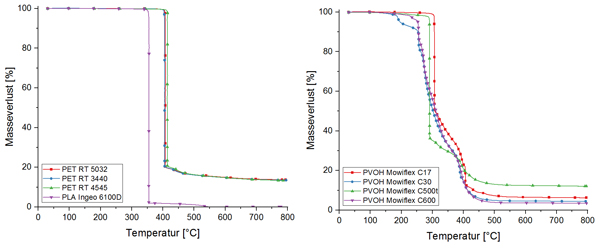
The tubular base structure was woven from polyester threads. Depending on the variant, cilia threads or a combination of cilia threads (piezoelectric PVDF or Nitinol threads) and conductor threads (silver-plated polyamide, Madeira HC40) were incorporated into the base fabric. The use of conductor threads was necessary when using electroactive PVDF multifilament threads or short fibres to stimulate cilia movement. When using one-way or two-way shape memory (SM) filaments as cilia material, no separate conductor filaments had to be incorporated into the fabric, as the SM filaments were directly contacted and conductive in order to initiate the movement of the cilia.
Development of biomimetic support structures
The human trachea has approximately 15 to 20 tracheal cartilages. They are horseshoe-shaped, have a diameter of 20 mm, with the open side facing dorsally (towards the back), and are approximately 4 mm wide and 1 mm thick. Their outer surface is flat and the inner surface is convex. Tracheal cartilages that can be integrated into the web (cartilage clips/support structures) should be manufactured using 3D printing and should be able to withstand a compression force of at least 1.2 N.
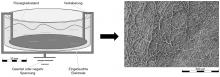
Based on this geometry, a total of 10 different models were developed. The differences in geometry resulted from variations in the leg geometry (C- and U-shaped), wall thickness and radius. The support structures were produced using photopolymer printing based on the stereolithography concept with an Objet 30 Prime from Stratasys in order to achieve the necessary geometric details. Exemplary structures are shown in Figure 1.
To examine the cartilage structures, clamps that meet the requirements for commercially available measurement technology were developed, designed and implemented using 3D printing. The clamps developed enable pressure loading in various anatomical positions of the cartilage segments (anterior-posterior & medial-lateral).
Integration of support structures into the tissue structure
Based on the previously presented woven tubular fabric, including the naps anchored in the base fabric on the fabric surface, a weaving structure was developed that could accommodate and fix the developed support structures at defined intervals in the base fabric. The integration of the support structures was achieved by weaving a fabric pocket over the entire circumference of the fabric. The dimensions (width and thickness) of the fabric pocket were adapted to those of the support structures, which were fixed between two layers of fabric and secured against slipping and "twisting out" of the structure. The number of support structures per defined fabric length was adjustable in terms of binding, and different clip widths could also be integrated into the tubular fabric by adjusting the fabric pocket size. The implemented demonstrator is shown in Figure 3. The inward-facing cilia and tissue pockets with the integrated support structures are clearly visible.
Textile physical analysis of the support and tissue structures as well as movement analysis
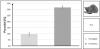
The average tensile strength of the human trachea is approximately 230 N [8]. The tubular tissue structures with integrated support structures exhibited a maximum tensile strength of approximately 4300 N. A yield strength of approximately 1400 N was determined. This means that the mechanical requirements of the human trachea are fully met. All support structures developed to prevent the trachea from collapsing exhibited a compression force greater than 1.2 N. In some cases, the target value was exceeded tenfold.
In addition, the influence of repeated or cyclic tensile loading on the position of the support structures integrated into the tissue was investigated. To this end, a load cycle test with 150 cycles was performed, in which a tensile load of up to a maximum force of 230 N (target value) was repeatedly applied, followed by relief to the initial position. A sample holder was developed and implemented for this purpose so that the tubular structure was loaded biomimetically across the entire cross-section. The results show that the support structures woven into the tissue pockets remained firmly fixed and did not "twist out" in the circumferential direction. The selected integration and fixation method thus ensures permanent positional stability under cyclic loading.
Motion analysis of the various patterns showed that PVDF fibres did not enable ciliary movement. However, the SM filaments with a two-way effect demonstrated repeatable ciliary movement. This approach can be used in the future to replicate the functioning of human cilia. As a further alternative approach, fabrics with parallel conductor threads were flocked with polyamide short fibres. Using an alternating electric field, intermittent cilia movement could also be simulated here.
Summary
A novel tracheal implant was developed at ITM that excellently replicates the macroscopic structure of the human trachea. The developed structure could be manufactured using commercially available shuttle weaving technology without any design modifications. To maintain a pressure-stable tubular structure, 3D-printed support structures were integrated into tissue pockets. Production can be carried out integrally and can be adapted to individual patients in terms of tissue length, support structure spacing, number of support structures and pressure stability. In addition, various concepts were investigated to replicate the microscopic structure in order to generate mass transport. The basis for this was the creation of polnop tissue and the use of piezoelectric PVDF fibres. It was found that PVDF nubs did not allow for movement on a microscopic scale. Ciliary movement was achieved using other actuator fibres such as nitinol fibres. Ciliary movement can also be achieved using flock fibres.
Acknowledgements
The project ‘Tubular tissues with rigid and flexible structural zones and mass transport for the biomimetic construction of the trachea (01IF22889N)’ is funded by the Federal Ministry for Economic Affairs and Energy as part of the ‘Industrial Collective Research (IGF)’ programme on the basis of a resolution passed by the German Bundestag.
References
[1] Aleksanya, A.; Stoelben, E.: Laryngotracheal resection as an alternative to permanent tracheostomy. Pneumologie 73 (2019), No. 4, pp. 211–218. URLhttps://www.thieme-connect.com/products/ejournals/html/10.1055/a-0809-0232
[2] Udelsma, Brooks; Mathisen, Douglas J.; Ott, Harald C.: A reassessment of tracheal substitutes—a systematic review. In: Annals of Cardiothoracic Surgery 7 (2018), No. 2, pp. 175–182. URLhttps://www.annalscts.com/article/view/16458/16661
[3] BVMe d: BVMed provides information on tracheotomy and laryngectomy care. URL https://www.bvmed.de/verband/presse/pressemeldungen/bvmed-informiert-ueber-tracheotomie-und-laryngektomie-versorgung. – Update date: 19 May 2016 – Review date: 15 October 2025
[4] Canzan, F.; Aggazzotti Cavazza, E.; Mattioli, F.; Ghidini, A.; Bottero, S.; Presutti, L.: Step-by-Step Tracheal Resection with End-to-End Anastomosis. In: Ghidini, Angelo; Mattioli, Francesco; Bottero, Sergio; Presutti, Livio (eds.): Atlas of Airway Surgery : ACham: Springer International Publishing, 2017, pp. 75–82
[5] Weme, Richard D.; Detamore, Michael; Weatherly, Robert A.: Immunohistochemical characterisation of rabbit tracheal cartilages. In: Journal of Biomedical Science and Engineering 03 (2010), No. 10, pp. 1007–1013
[6] Damian o, Giuseppe; Palumbo, Vincenzo Davide; Fazzotta, Salvatore; Curione, Francesco; Lo Monte, Giulia; Brucato, Valerio Maria Bartolo; Lo Monte, Attilio Ignazio: Current Strategies for Tracheal Replacement: A Review. In: Life 11 (2021), No. 7, pp. 618. URLhttps://www.mdpi.com/2075-1729/11/7/618
[7] Rettinge, Gerhard; Hosemann, Werner; Hüttenbrink, Karl-Bernd; Werner, Jochen Alfred: ENT Surgery : . 5th, completely revised edition. Stuttgart: Thieme, 2018
[8] A. Berghau s: . In: Cardiac, Thoracic and Vascular Surgery 1987 (1987), Volume 1. URL https://epub.ub.uni-muenchen.de/6218/1/6218.pdf – Review date 2025-10-15
Technische Universität Dresden
Fakultät Maschinenwesen
Institut für Textilmaschinen und Textile Hochleistungswerkstofftechnik (ITM)
01062 Dresden













![Abbildung 1: Prozess der systematischen Literaturrecherche nach [Yu 17]](/sites/default/files/styles/medium/public/2025-02/Abbildung%201%20_0.jpg?itok=Ls_2OQlL)